Эпинефрин(адреналин) является катехоловым нейромедиатором и гормоном, широко используемым при приготовлении таких лекарств, как сердечная реанимация, бронхоэктазы, анафилаксия и урокиназа. При клиническом применении обычные способы получения в основном включают биологические способы, химические способы и способы биосинтеза. В этой статье будут проанализированы эти методы подготовки.
1. Биологический метод:
В биосинтезе адреналина в качестве предшественника обычно используется тирозин, который вырабатывается в результате многочисленных реакций, катализируемых ферментами. Синтез и катализ этих ферментов регулируются различными факторами, такими как гормоны, нейротрансмиттеры и лекарства.
1) Превращение тирозингидроксилазы в ДОФА:
Первыми синтезированными соединениями были фенолкарбоновые кислоты.
Фенольная карбоновая кислота превращается в 3,4-дигидроксифенилаланин (ДОФА) под действием тирозингидроксилазы. Этот ответ регулируется гормоном дофамином и его производными, нейротрансмиттерами или нейрофармацевтическими препаратами.
2) ДОФА окисляется с образованием дофамина:
ДОФА-декарбоксилаза также окисляет ДОФА до дофамина с помощью фермента, опосредованного синтезом дофамина.
3) N-метилтрансфераза побуждает дофамин генерировать норадреналин:
Норадреналин превращается в адреналин под действием дофамин-N-метилтрансферазы.
Методы, обычно используемые в биологических методах, включают белковую инженерию и генную инженерию.
2. Химический метод:
В химическом синтезе тирозин и формальдегид образуют метил-ДОФА (реактив Максвелла) в результате реакции 1,4-присоединения. Метил-ДОФА разлагается при 60 градусах путем декарбоксилирования с образованием адреналина.
Химический синтез адреналина в основном включает следующие реакции:
1) добавление тирозина и формальдегида по Михаэлю
Тирозин и формальдегид подвергаются реакции присоединения 1,4-Михаэля в подходящих условиях реакции с образованием промежуточного соединения метил-ДОФА.
2) Декарбоксилирование
Промежуточное соединение метил-ДОФА разлагается при высокой температуре в результате реакции декарбоксилирования с образованием адреналина.
К преимуществам химического синтеза адреналина относятся отсутствие связи с биокатализом, высокая эффективность синтеза и возможность получения различных производных адреналина посредством структурных изменений. Однако химический метод также имеет недостатки, такие как сложность процесса и высокая стоимость.
3. Биосинтез:
Биосинтетический синтез адреналина в основном осуществляется с использованием технологии микробного синтеза. Отсеивая и модифицируя микробные штаммы, они могут производить адреналин.
Обычные продуцирующие штаммы микробов-хозяев для рекомбинации генов включают Escherichia coli, Saccharomyces cerevisiae, Trichoderma и т. д., и синтез адреналина путем рекомбинантной экспрессии Escherichia coli является более популярным способом. Суть метода заключается в том, чтобы вывести метаболический путь тирозина из клетки, а затем культивировать его метаболический путь в контейнере, чтобы он мог производить большое количество адреналина. Большая часть этого подхода автоматизирована и легко масштабируется.
4. Вывод:
Биологические методы, химические методы и методы биосинтеза являются обычными методами получения адреналина. Биологический метод действительно может генерировать естественный адреналин с точки зрения физиологии и фармакологии и может обеспечить естественные лекарственные эффекты, но он регулируется генами и ферментами, что затрудняет его приготовление; химические и биосинтетические методы обладают высокой эффективностью и высоким выходом. , Высокая характеристика и модификация характеристик, но химический процесс является громоздким и дорогостоящим, а метод биосинтеза трудно поддерживать эффективность, но он может эффективно координировать микробный рост и метаболизм для массового производства.

Эпинефрин (эпинефрин), нейротрансмиттер и гормон, также является важным лекарственным средством. Он производит физиологические эффекты, связываясь с адренергическими рецепторами. Эпинефрин включает производные амфетамина и катехоламинов и обычно используется для лечения таких состояний, как астма, учащенное сердцебиение и тяжелые аллергические реакции. Кроме того, препарат также используется в процессе оказания первой помощи и родовспоможения.
Химическая реакция эпинефрина включает взаимодействие нескольких химических частей, поэтому в этой статье будет представлена роль этих частей в химической реакции.
Химическая структура:
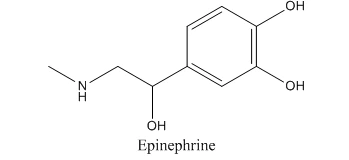
Во-первых, представлена химическая структура адреналина. Молекула эпинефрина состоит из структуры фенилэтиламина и кольцевой структуры катехола, аббревиатура — Эпи. Имеется два хиральных атома углерода, расположенных в позициях и соответственно. Следовательно, эпинефрин существует в четырех стереоизомерах, а именно (R,R)-Epi, (S,S)-Epi, (R,S)-Epi, (S,R)-Epi. Среди них только (R,R)-Epi является изомером с сильной физиологической активностью, который также является основным изомером, продуцируемым in vivo.
Реакция адреналина с ионами водорода:
В бензольном кольце эпинефрина есть гидроксильные и аминные группы, поэтому он имеет определенную кислотность и щелочность. При взаимодействии адреналина с ионами водорода (Н++) могут протекать следующие реакции:
Эпи плюс Н ^ плюс → Эпи Н ^ плюс
Это критическая реакция, потому что EpiH^ plus является продуктом ионизации адреналина, что влияет на его физиологические и фармакологические свойства.
Реакции окисления эпинефрина:
Гидроксильные и амфетаминовые группы адреналина обладают очевидными окислительно-восстановительными свойствами и могут вступать в реакции окисления. Когда адреналин вступает в контакт с кислородом, могут возникнуть следующие реакции:
Эпи плюс О2→ ЭпиО2
Кроме того, когда эпинефрин вступает в контакт с некоторыми окислителями, такими как перекись водорода, также может возникнуть реакция окисления.
Кислотно-щелочная реакция Эпинефрина:
Гидроксильные и аминогруппы адреналина также являются кислотными и основными, и они могут вызывать сложные кислотно-щелочные реакции при различных значениях рН. Когда значение pH ниже, чем значение pKa соединения (3,5 и 9,0), тогда гидроксильная группа будет протонирована, что приведет к сильной кислоте Льюиса EpiH^ plus ; и наоборот, когда значение pH выше pKa, аминогруппа будет депротонирована, Epi^- дает сильное основание Льюиса. Это взаимодействие кислотных свойств и pH оказывает значительное влияние на эффективность и побочные эффекты эпинефрина в медицинских целях.
Реакция азотной газификации эпинефрина:
Аминогруппа в эпинефрине также может подвергаться реакции азотирования при воздействии определенных химических реагентов из-за окислительно-восстановительных свойств. Например, когда адреналин вступает в контакт с нитратом ртути, он вызывает темно-синюю химическую реакцию:
Эпи плюс Hg(НЕТ3)2→ HgO2N-эпи плюс 2HNO3
Выше приведены несколько типичных типов химических реакций адреналина, и каждая его часть играет разные роли в реакции. Характеристики и свойства химических реакций оказывают важное влияние на фармакологические эффекты и медицинские применения адреналина, а также служат руководством и идеями для химиков и фармакологов по разработке более эффективных лекарств.

